新一代CGT疗法,引领生物制药的新浪潮
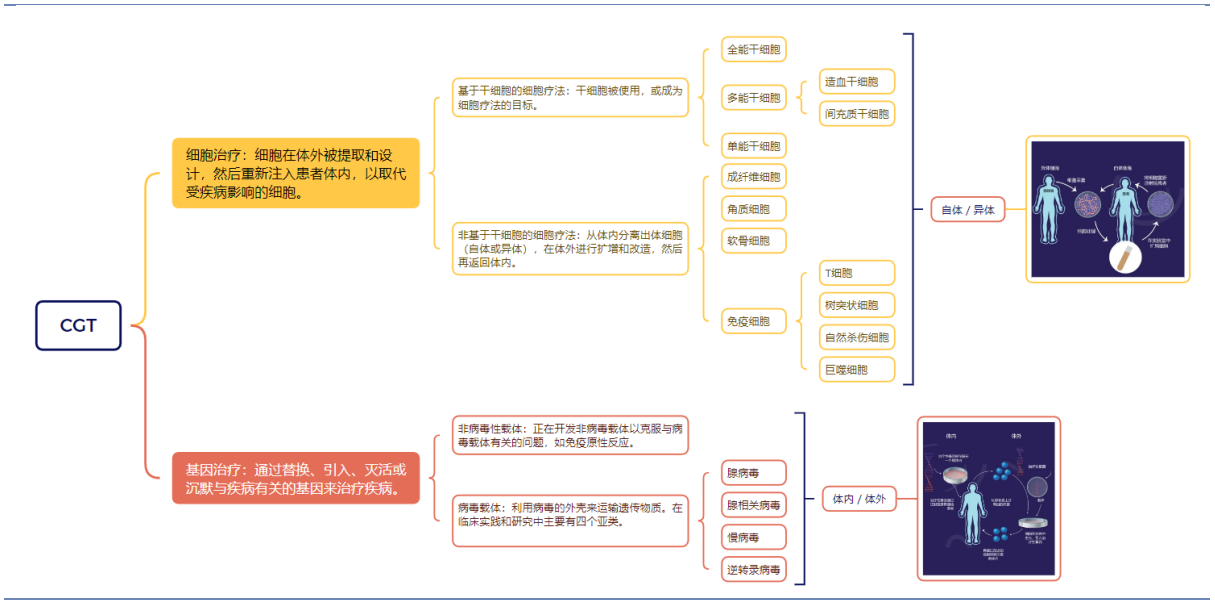
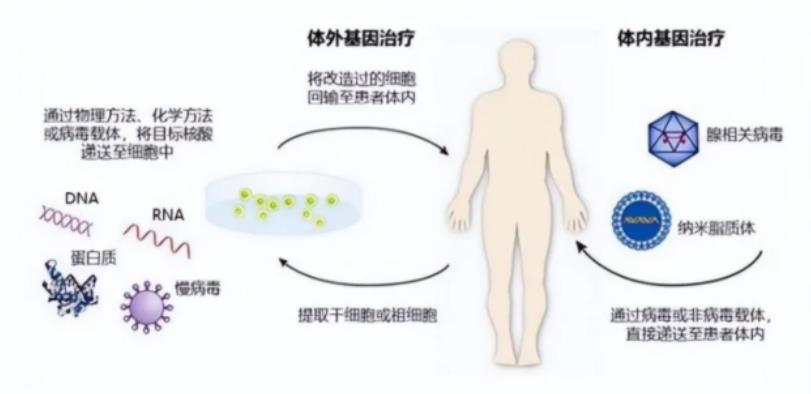
细胞基因治疗(CGT,Cellular and Gene Therapy)是目前生物医药领域最具前景的发展方向。CGT疗法是继小分子、大分子靶向疗法之后的新一代精准疗法,引领生物制药的新一轮浪潮。CGT是指利用基因表达和体外改造等手段,将确定的遗传物质转移至患者的特定靶细胞内,通过基因添加、基因修正、基因沉默等方式修饰个体基因的表达或修复异常基因,进而实现治疗的方法具体分为细胞治疗和基因治疗。
基因治疗发展史
-
1972年Friedmann和Roblin首次提出基因治疗的概念;
-
2003年全球首个基因治疗药物重组人p5腺病毒注射液(商品名:今又生/Gendicine)在中国获批;
-
2005年由腺病毒改造而来的溶瘤病毒治疗产品安柯瑞(Oncorine)在中国获批上市为全球第一个获批的溶瘤病毒药物;
-
2012年基于AAV的基因治疗药物GIybera获EMA批准上市;
-
2015年Amgen 公司的黑色素瘤治疗药物Imlygic成为FDA和 EMA批准的首款溶瘤病毒治疗产品。
-
2017年以来,随着Kymriah、Luxturna、Zolgensma等里程碑产品获FDA批准上市,基因治疗持续取得突破性进展,成为最具发展潜力的全球性前沿医药领域之一。
2019年以来,国内基因治疗行业加快发展,CAR-T产品、溶瘤病毒产品、AAV产品等基因治疗临床试验持续增加,NMPA亦于 2021年6月和9月批准中国首款CAR-T产品奕凯达,以及中国首个1类新药CAR-T产品倍诺达®。2024年 12月首个获 FDA批准的间充质干细胞(MSC)疗法Ryoncil(remestemcel)上市。2025年1月中国附条件批准铂生卓越的间充质干细胞疗法艾米迈托赛注射液。
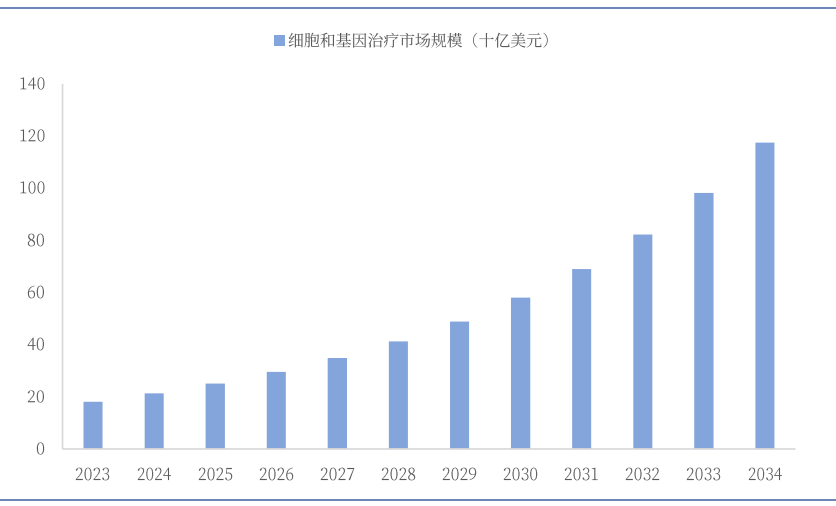
CGT市场快速扩容
根据Precedence Research预测,2024年全球细胞和基因治疗市场规模为212.8亿美元,预计到2034年将达到1174.6亿美元左右,从2024年到 2034年的复合年增长率为18.6%。其中,2023年北美细胞和基因治疗市场规模约为90亿美元,占比约50%。
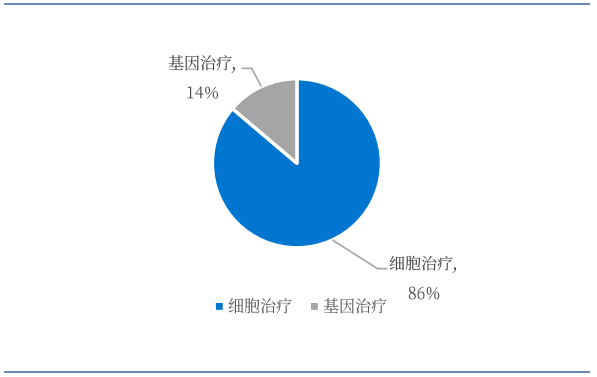
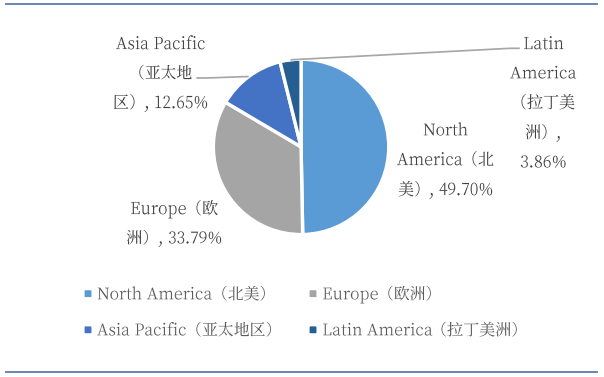
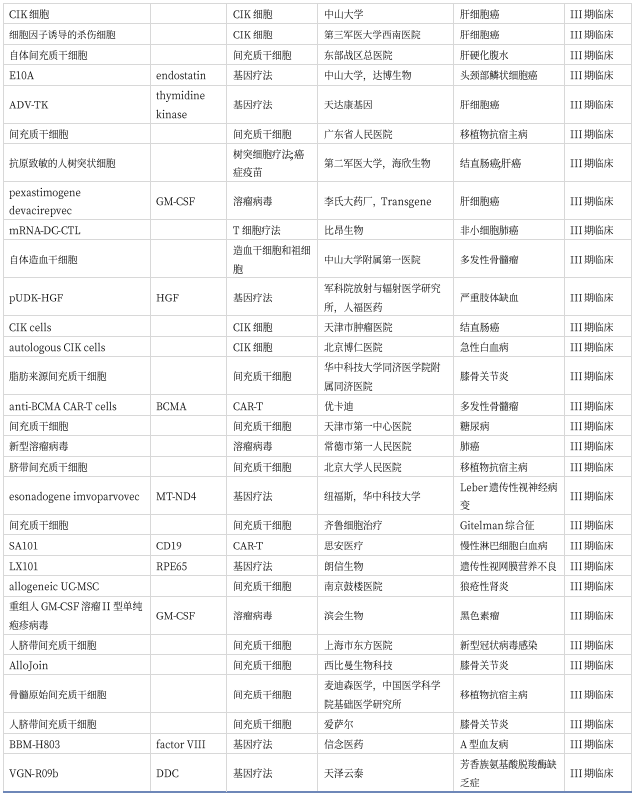
CGT上市品种盘点
全球已有超70款CGT品种上市,包括CAR-T疗法、干细胞疗法、溶瘤病毒疗法、组织疗法和基因疗法等。
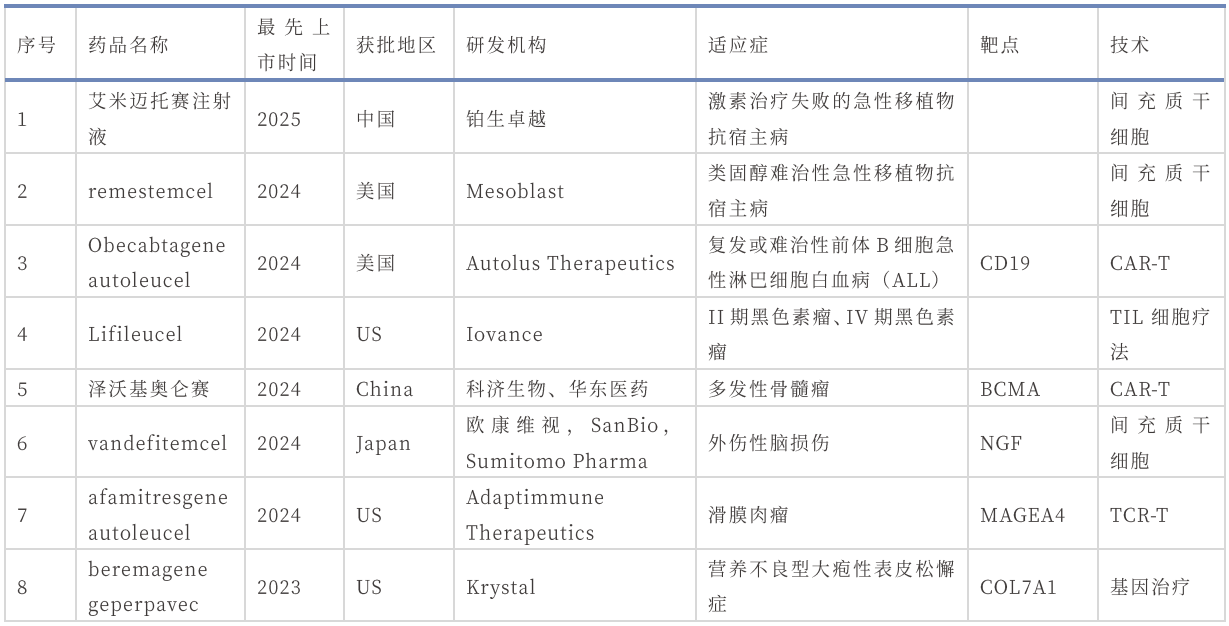
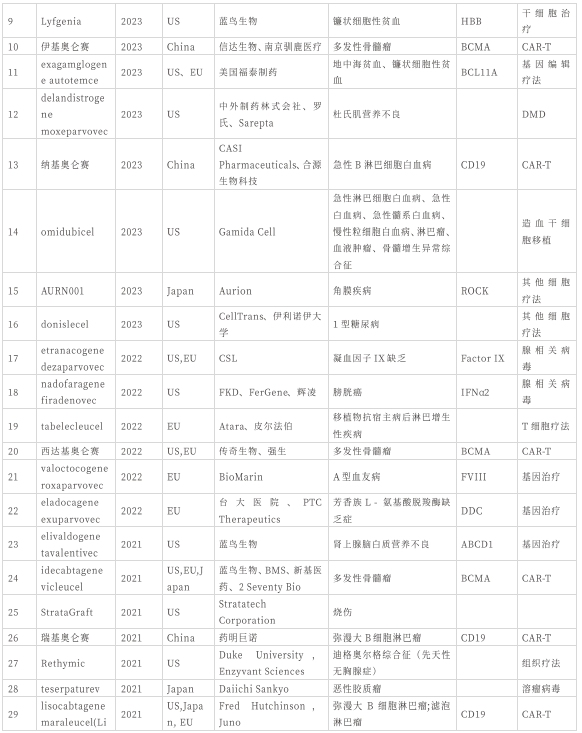
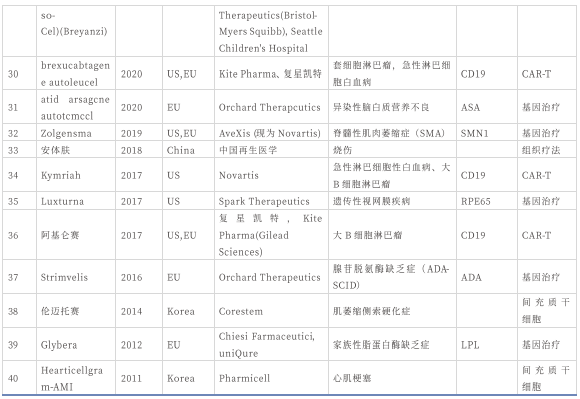
中国基因治疗产品盘点
中国CGT临床三期以上产品已达40多款,其中6款CART获批上市,另有5款产品申报上市。随着国内研发投入的增加和技术不断成熟,预计将有更多的产品在中国市场获批。