《医疗器械分类目录》调整,“水光针”等医美产品被纳入III类医疗器械管理。3月30日,国家药监局调整《医疗器械分类目录》(下简称《目录》),其中涉及医疗美容领域的调整内容包括:
(1)将俗称“水光针”的一类产品纳入III类医疗器械管理,并进一步明确产品成分、用途等;
(2)明确射频治疗仪按照III类医疗器械监管;
(3)新增“整形用植入线材”类别并按III类医疗器械管理。
本次《目录》调整,明确了部分医美产品的定位、规范,将推动行业进一步规范发展。

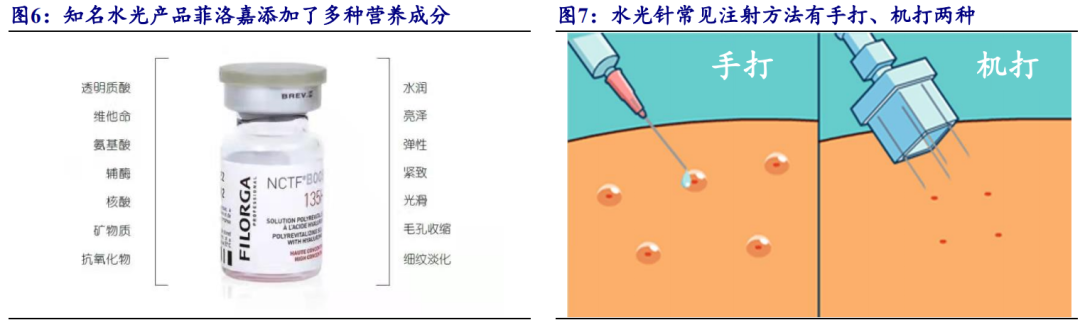
“水光针”通常是指代一类以无交联或低交联小分子透明质酸钠为主要成分,并添加维生素、氨基酸、矿物质等多种成分的复合溶液。其中,透明质酸钠主要起补水、保湿作用,其余成分则用于满足美白、抗衰、除皱等需求。“水光针”需注射至真皮层内才能起到治疗效果,常见注射方法有手打、机打两种:手打水光可根据实际情况控制深浅,但依赖医生操作技术;机打水光给药均匀、力度平稳,但易造成漏液浪费。水光针效果可维持 3-6个月,因此水光针消费者通常一年内会购买 2-3 次。
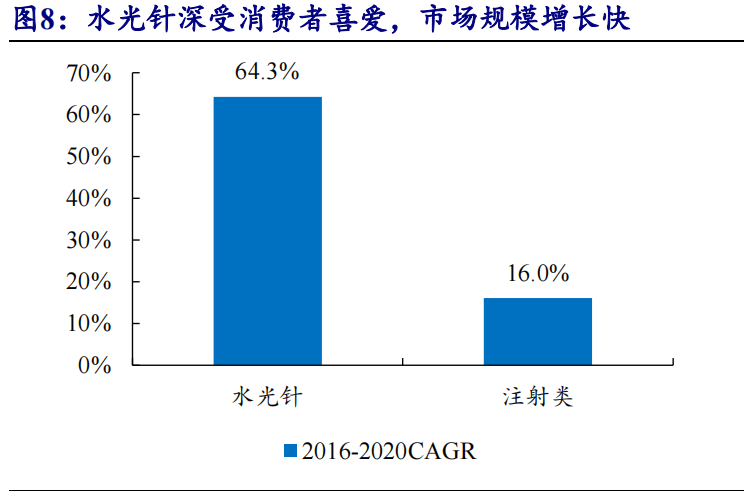
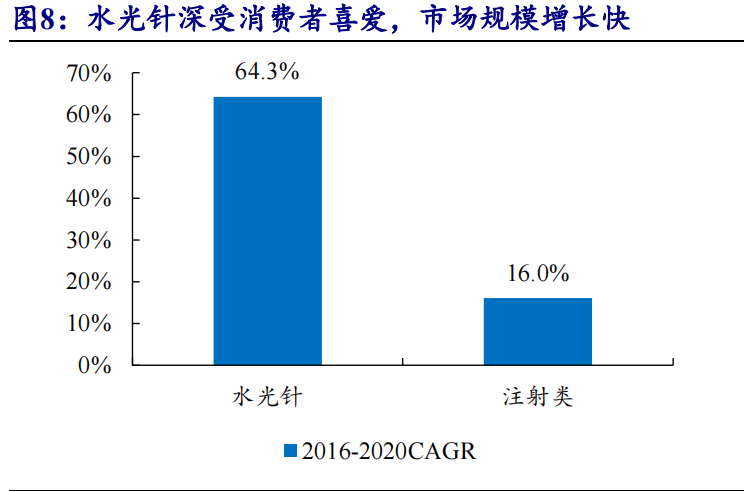
水光针由于价格低、功效多样、恢复期短,长期以来深受消费者喜爱。根据亿渡数据,我国水光针项目市场规模2016-2020年复合增速达到 64.3%,远超注射类医美项目整体增速(仅16.0%)。但目前水光针市场存在大量不合规现象:一方面,多数用于注射的产品均未取得III类医疗器械注册证,例如,知名水光产品实际为妆字号,按规定仅能用于涂抹,不能用于注射;另一方面,由于水光针操作简单,很多未持有医疗机构执业许可证的美容院也可能为了牟利违规操作注射,带来较大安全隐患。
行业乱象倒逼监管加强,水光针纳入“正规军”影响深远。
本次《目录》调整对医美行业各参与者均会产生影响:(1)从医美机构角度看,严监管下,机构将减少不合规产品使用,作为替代,短期将推动相关合规产品的采购需求;(2)从厂商角度看,水光针定位明确后,各大厂商将积极推动产品申报,力争尽早拿证推出产品,享受合规市场红利期;(3)从消费者角度看,本次《目录》调整结合近期315晚会等对黑医美的曝光,也将教育、警醒消费者,进一步推动医美行业规范化。目前市场上具备水光针类似替代功能且拥有III类证书的合规产品,主要包括冭活泡泡针(爱美客)、嗨体2.5(爱美客)、润致娃娃针(华熙生物)和瑞蓝唯瑅(高德美)等,但上述产品在适应症、注射部位等方面仍与现出台的水光针要求存在一定差异。